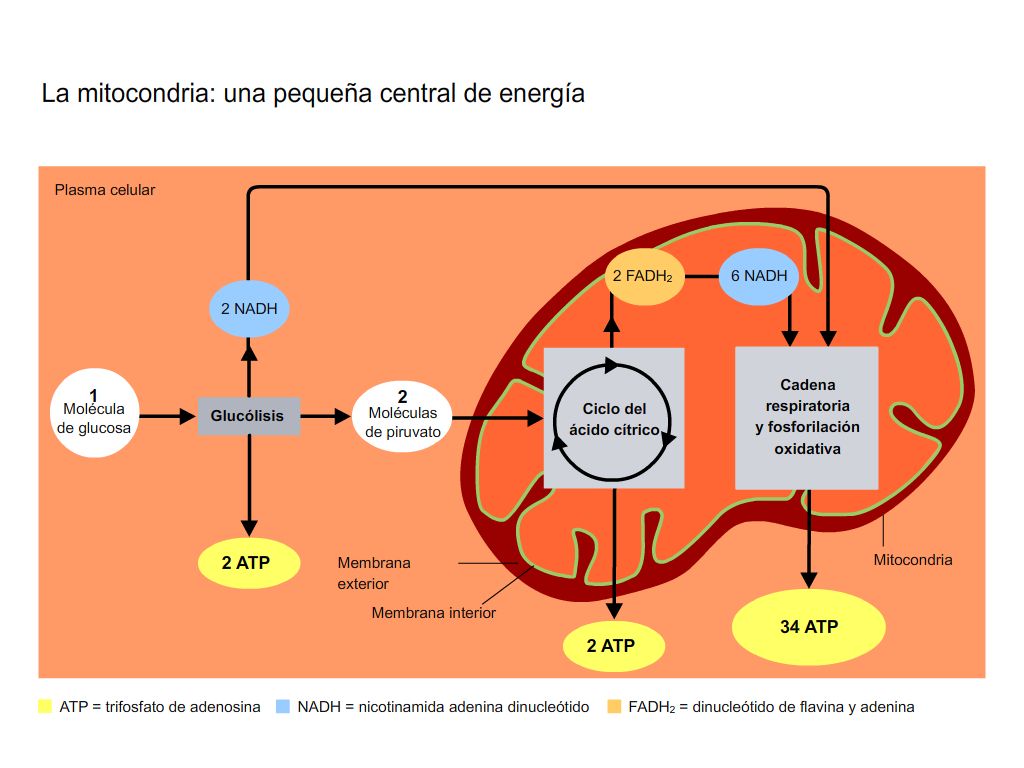
La energía requerida para iniciar una reacción es esencial en los procesos químicos
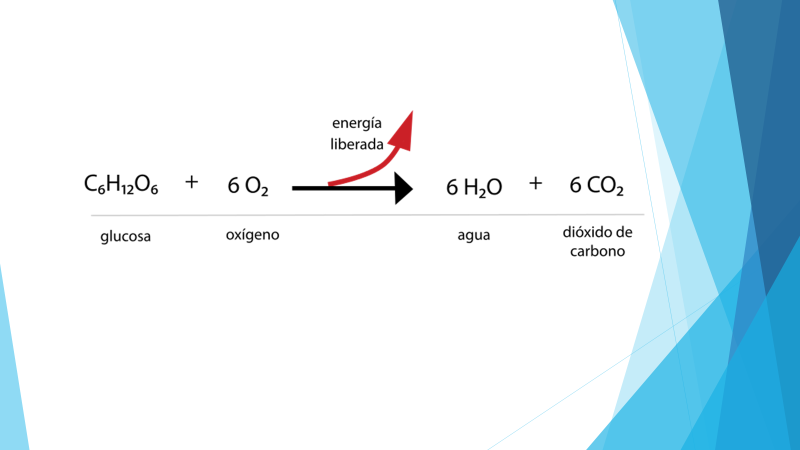
La energía requerida para iniciar una reacción química juega un papel fundamental tanto en la química como en diversas aplicaciones industriales y biológicas. Esta energía, comúnmente conocida como energía de activación, es el umbral que las moléculas deben superar para que se produzcan reacciones químicas. Sin esta energía, las moléculas reaccionantes no podrían alcanzar el estado de transición necesario para que ocurra la transformación química, lo que limita la velocidad a la que pueden llevarse a cabo las reacciones y, en consecuencia, afecta la productividad en muchas industrias. Comprender el concepto de energía de activación es vital no solo para químicos, sino también para ingenieros, biólogos y profesionales de diversas disciplinas que se relacionan con mecanismos de reacción y cinética.
La energía de activación no es un concepto aislado, sino que está relacionado con otras variables importantes, como la temperatura y la concentración de los reactivos. A medida que aumenta la temperatura, las moléculas obtienen más energía cinética, lo que significa que muchas más de ellas podrán alcanzar el umbral de energía de activación de la reacción. Además, el entorno en el que ocurre la reacción, incluyendo la presencia de catalizadores, puede facilitar o dificultar el proceso. En esta exploración, revisaremos la definición de energía de activación, los factores que influencian su magnitud y las implicaciones que tiene en el ámbito industrial y biológico.
Definición de energía de activación en reacciones químicas
La energía de activación es la cantidad mínima de energía necesaria para que las moléculas de reactivos inicien una reacción. Este concepto se deriva de la teoría de colisiones, que establece que las partículas deben colisionar con suficiente energía y en la orientación correcta para que ocurra una reacción. En este sentido, la energía de activación actúa como una barrera que los reactivos deben superar para transformarse en productos. Esta barrera puede ser visualizada en un gráfico de energía versus el progreso de la reacción, donde se observa una subida inicial (la energía de activación) seguido de una caída al nivel de energía de los productos.
Es importante señalar que la energía de activación no es un valor fijo; varía entre diferentes reacciones y está influenciada por una variedad de factores. Por ejemplo, una reacción que involucra la ruptura de enlaces fuertes normalmente tendrá una energía de activación más alta que una reacción en la que se forman enlaces más débiles. Por lo tanto, el estudio de la energía de activación es crucial para comprender no solo el ritmo de las reacciones, sino también las condiciones bajo las cuales estas pueden ser optimizadas y controladas.
La relación entre energía de activación y velocidad de la reacción
La relación entre la energía de activación y la velocidad de una reacción se puede describir a través de la ecuación de Arrhenius, que muestra que la velocidad de una reacción aumenta exponencialmente a medida que disminuye la energía de activación. Esto implica que pequeñas variaciones en la energía de activación pueden conducir a significativas diferencias en la tasa de reacción. En términos generales, una reacción con una energía de activación baja ocurrirá más rápidamente que una con una energía de activación elevada. Por lo tanto, la manipulación de la energía de activación se convierte en un elemento crucial en el diseño de procesos químicos eficientes.
En la práctica, los ingenieros y químicos a menudo buscan métodos para reducir la energía de activación de forma eficaz. Esto puede lograrse mediante el uso de catalizadores, que son sustancias que aumentan la tasa de reacción sin ser consumidas en el proceso. Los catalizadores funcionan proporcionando un camino alternativo para la reacción, uno que tiene una energía de activación más baja. Esto permite que más moléculas de reactivos alcancen el umbral necesario para reaccionar, lo que acelera la reacción sin alterar la energía total del sistema.
Catalizadores y su influencia en la energía de activación
Los catalizadores son herramientas esenciales en la química moderna, y su capacidad para disminuir la energía de activación es fundamental en muchos procesos industriales. Por ejemplo, en la producción de amoníaco, se utilizan catalizadores para facilitar la reacción entre el nitrógeno y el hidrógeno, que de otro modo sería muy lenta a temperaturas normales. Al reducir la energía de activación, los catalizadores permiten que esta reacción progrese a temperaturas y presiones más bajas, lo que no solo ahorra energía, sino que también mejora la seguridad y la viabilidad económica de los procesos.
Es importante tener en cuenta que los catalizadores no alteran el equilibrio de la reacción, es decir, no cambian las energías relativas de los reactivos y productos. Simplemente, crean un camino alternativo para facilitar la reacción. Sin embargo, la eficacia de un catalizador puede depender de diversos factores, incluyendo su composición química, su estructura física y las condiciones operativas como la temperatura y la presión. Por lo tanto, la investigación y el desarrollo de nuevos catalizadores son áreas activas en la ciencia de materiales y la ingeniería química.
Factores que afectan la energía de activación
Además de la intervención de catalizadores, existen otros factores que pueden influir en la energía de activación de una reacción. Estos factores incluyen la temperatura, la presión y la naturaleza de los reactivos. Comprender cómo cada uno de estos elementos afecta la energía de activación es esencial para controlar y optimizar los procesos químicos.
La temperatura es quizás el factor más obvio que afecta la energía de activación. A temperaturas más altas, las moléculas tienen más energía cinética, lo que aumenta la probabilidad de que las colisiones entre reactivos generen suficiente energía para superar la barrera de activación. Esto es especialmente relevante en reacciones donde el tiempo de reacción es un factor crítico, como en la síntesis de productos químicos en la industria. Considerando esto, los químicos pueden ajustar la temperatura de un sistema para maximizar la velocidad de reacción y la producción.
Otro factor que influye en la energía de activación es la presión. En reacciones que involucran gases, aumentar la presión a menudo incrementa la frecuencia de colisiones entre moléculas, lo que puede disminuir la energía de activación efectiva. Este es un aspecto que se ha utilizado en la industria para aumentar la eficiencia de varias reacciones químicas.
La influencia de la naturaleza de los reactivos
Finalmente, la naturaleza de los reactivos también desempeña un papel importante en la determinación de la energía de activación. Algunas sustancias reactivas son inherentemente más propensas a reaccionar que otras debido a sus estructuras moleculares y la estabilidad de sus enlaces. Por ejemplo, los enlaces covalentes tienen diferentes energías, y los enlaces más fuertes requerirán más energía para ser rompidos durante una reacción. Esto significa que, al seleccionar reactivos para un proceso específico, los químicos deben tener en cuenta no solo la disponibilidad de los materiales, sino también la energía de activación y su impacto en la viabilidad del proceso.
Aplicaciones de la energía de activación en la industria
La comprensión de la energía de activación y el control de este parámetro son esenciales para muchas industrias, incluidas la farmacéutica, la petroquímica y la producción de alimentos. Las aplicaciones más notables se encuentran en la síntesis de compuestos químicos, donde el control de la energía de activación determina la eficiencia y la rentabilidad de los procesos.
En la industria farmacéutica, por ejemplo, la optimización de reacciones químicas es crucial en la producción de medicamentos. Los químicos buscan reducir la energía de activación en la síntesis de fármacos, no solo para mejorar el rendimiento, sino también para minimizar los procesos secundarios que pueden generar residuos nocivos. Esto implica un enfoque minucioso en la selección de reactivos y el uso estratégico de catalizadores.
En la industria petroquímica, la energía de activación es igualmente relevante. La refinación de petróleo y la producción de combustibles a menudo involucra reacciones complejas que requieren control preciso sobre la energía de activación para maximizar la producción de productos deseados mientras se minimizan subproductos no deseados. Aquí, la aplicación de técnicas de catálisis y el control de condiciones operativas son prácticas estándar.
El papel de la energía de activación en procesos biológicos
En el ámbito biológico, la energía de activación también juega un papel fundamental. Las enzimas, que actúan como catalizadores biológicos, reducen la energía de activación de las reacciones químicas dentro de los organismos. Esto permite que las reacciones metabólicas ocurran a temperaturas y condiciones compatibles con la vida, acelerando procesos vitales como la digestión y la síntesis de biomoléculas. Sin el papel de las enzimas y su capacidad para disminuir la energía de activación, muchas reacciones esenciales simplemente no podrían ocurrir a la velocidad requerida para sustentar la vida.
El estudio de cómo las enzimas afectan la energía de activación es crucial en áreas como la biotecnología y la medicina. Por ejemplo, la investigación en el desarrollo de enzimas específicas puede llevar a la mejora de procesos industriales, así como a la creación de terapias más efectivas en medicina personalizada. Así, la comprensión de la energía de activación no solo tiene implicaciones en la química, sino que también se extiende a campos interdisciplinarios que abarcan la biología y la ingeniería.
Conclusión
La energía requerida para iniciar una reacción, conocida como energía de activación, es un concepto clave en la comprensión de las reacciones químicas y sus aplicaciones. A medida que se exploran las diversas influencias como la temperatura, la presión y los catalizadores, se hace evidente que esta energía no solo determina la velocidad de las reacciones, sino que también influye en la eficacia de procesos en múltiples industrias. Desde la producción farmacéutica hasta la biotecnología, la energía de activación es fundamental para el desarrollo y la optimización de reacciones químicas. El estudio y la manipulación de este parámetro ofrecen oportunidades significativas para mejorar la sostenibilidad y la eficiencia en campos científicos y tecnológicos.
En última instancia, comprender la energía de activación proporciona una base sólida para la innovación en una variedad de disciplinas. Al reducir la energía de activación, utilizar catalizadores efectivos y controlar las condiciones de reacción, los profesionales pueden abordar desafíos complejos en la química y la biología que impactan tanto nuestra vida cotidiana como el entorno que nos rodea. La investigación en este ámbito sigue avanzando, prometiendo futuros desarrollos que podrían transformar nuestra comprensión y manejo de la química en el mundo moderno.





Deja una respuesta