
De qué manera ocupan los electrones los niveles de energía en los átomos
La estructura atómica es fundamental para entender la química y la física, ya que los electrones juegan un papel crucial en las propiedades de los elementos y sus interacciones. Cada átomo está compuesto por un núcleo central que alberga protones y neutrones, mientras que los electrones orbitan alrededor de este núcleo en niveles de energía específicos. Estos niveles de energía son críticos porque determinan cómo los electrones se distribuyen, cómo se comportan en las reacciones químicas y cuál será el resultado de estas interacciones. En este artículo, se explorará cómo los electrones ocupan estos niveles de energía, desde sus características fundamentales hasta las implicaciones de su distribución. Este análisis profundo permitirá comprender mejor los conceptos de energía, enlace químico y reactividad de diferentes átomos y moléculas.
A medida que profundizamos en el comportamiento de los electrones en los niveles de energía, es importante destacar que estas capas de energía no son discretas e independientes. De hecho, la teoría cuántica ha revolucionado nuestra comprensión de cómo se organizan los electrones en torno a un núcleo atómico. Cada nivel de energía puede alojar una cantidad específica de electrones, dependiendo de su configuración y de las reglas que rigen su comportamiento a nivel microscópico. Por lo tanto, la ocupación de los niveles de energía no solo está definida por la cantidad de electrones presentes, sino también por su configuración relativa y el tipo de interacciones que pueden ocurrir entre ellos.
Estructura de los niveles de energía
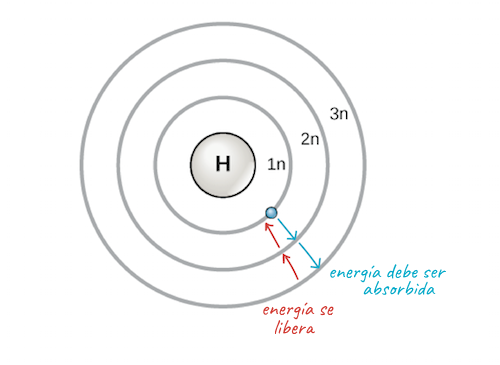
Los niveles de energía en los átomos se pueden entender a través del modelo atómico de Bohr, que establece que los electrones se mueven en órbitas discretas alrededor del núcleo. Según este modelo, cada órbita corresponde a un nivel de energía definido, y los electrones pueden saltar entre estos niveles mediante la absorción o emisión de energía. Un punto clave a considerar es que los niveles de energía son cuantizados, lo que significa que solo ciertos valores de energía son posibles. Esta característica define la estabilidad y la estructura de los átomos.
Principios de la mecánica cuántica
La mecánica cuántica ofrece un marco más completo que el modelo de Bohr y proporciona una descripción detallada de cómo los electrones ocupan los niveles de energía. Dentro de este contexto, los electrones no se describen como partículas que siguen trayectorias bien definidas, sino más bien como nubes de probabilidad. Estas nubes, llamadas orbitales, representan la amplitud de la probabilidad de encontrar un electrón en una región del espacio determinada. Cada orbital tiene una forma y una energía específicas, y pueden estar ubicados en diferentes niveles de energía.
Configuración electrónica
La manera en que los electrones llenan los niveles de energía se describe generalmente a través de la configuración electrónica. Esta configuración explica cómo se distribuyen los electrones entre los diferentes orbitales y niveles de energía. Cada elemento químico tiene una configuración electrónica única que determina sus propiedades y su comportamiento en reacciones químicas.
Los niveles de energía se organizan jerárquicamente en una serie de capas, que se dividen en subniveles que pueden variar según la energía. Por ejemplo, el primer nivel de energía (n=1) puede tener un subnivel s, el segundo nivel (n=2) puede tener subniveles s y p, y así sucesivamente. Cada subnivel puede contener un número limitado de electrones, que se asignan según los principios de exclusión de Pauli y el principio de Hund.
Reglas que rigen la ocupación de niveles de energía
La ocupación de los niveles de energía por los electrones se rige por una serie de reglas establecidas en la mecánica cuántica. Estas reglas no solo afectan el número de electrones que pueden ocupar un nivel de energía, sino también cómo se distribuyen, lo que tiene un impacto significativo en las propiedades químicas y físicas de los elementos. A continuación, se mencionan algunas de las reglas más relevantes:
- Principio de Exclusión de Pauli: Establece que no pueden existir dos electrones en un átomo con el mismo conjunto de números cuánticos. Esto significa que cada orbital solo puede albergar dos electrones con spins opuestos.
- Regla de Hund: Los electrones tienden a ocupar orbitales equidistantes antes de emparejarse. Esto maximiza el número de electrones con spins paralelos y, por lo tanto, reduce la repulsión electrostática entre ellos.
- Principio de Aufbau: Los electrones ocupan los niveles y orbitales de menor a mayor energía. Este principio guía la formación de la configuración electrónica en átomos en estado fundamental.
El cumplimiento de estas reglas permite una distribución `óptima` de los electrones en los niveles de energía, lo que contribuye a la estabilidad del átomo y sus propiedades reactivas. La comprensión de estas reglas es crucial para la predicción de los comportamientos químicos de los átomos en diversas condiciones.
Ejemplos de ocupación de electrones en niveles de energía
Para ilustrar la ocupación de electrones en niveles de energía, consideraremos algunos ejemplos de elementos comunes de la tabla periódica. Estos ejemplos ayudarán a visualizar cómo se aplica la teoría en la práctica y comprender la diversidad de configuraciones electrónicas entre diferentes elementos.
Ejemplo del Hidrógeno
El hidrógeno, el elemento más simple, tiene un solo electrón que ocupa el primer nivel de energía. Su configuración electrónica se expresa como 1s1, lo que indica que hay un electrón en el orbital 1s. Esta configuración simple tiene implicaciones significativas, como su reactividad en la formación de enlaces químicos.
Ejemplo del Carbono
El carbono es un elemento fundamental en la química orgánica y tiene seis electrones (configuración electrónica 1s2 2s2 2p2). En este caso, los dos primeros electrones llenan el primer nivel de energía, mientras que los cuatro restantes se distribuyen en el segundo nivel de manera que sigue la regla de Hund. Esta distribución permite que los electrones del carbono se relacionen favorablemente con otros átomos, formando enlaces covalentes que son vitales para la existencia de compuestos orgánicos.
Ejemplo del Oxígeno
El oxígeno, otro elemento esencial para la vida, tiene ocho electrones (configuración electrónica 1s2 2s2 2p4). Aquí, los dos electrones del primer nivel de energía ocupan el subnivel 1s, y en el segundo nivel, dos electrones llenan el subnivel 2s mientras que cuatro ocupan el subnivel 2p de manera que maximiza el spin. Esta disposición significa que el oxígeno es altamente electronegativo y puede formar enlaces fuertes con otros elementos, explicando su reactividad.
Conclusiones sobre la ocupación de electrones en los niveles de energía
El estudio de cómo los electrones ocupan los niveles de energía en los átomos es fundamental para comprender la estructura atómica y sus implicaciones en la química. La ocupación de electrones determina no solo las propiedades físicas de los elementos, sino también su comportamiento en las reacciones químicas. Comprender cómo estos niveles de energía son organizados y ocupados por los electrones proporciona una base sólida para el estudio de la química y sus interacciones, así como para la física atómica.
A medida que avanzamos en el conocimiento de la química moderna, los conceptos relacionados con los niveles de energía y la distribución de electrones siguen expandiéndose. La investigación en física y química cuántica nos brinda la oportunidad de descubrir nuevos materiales y tecnologías que podrían tener un impacto significativo en nuestra sociedad. Por lo tanto, la ocupación de electrones en los niveles de energía no solo nos ayuda a entender el mundo a nuestro alrededor, sino que también abre la puerta a innovaciones futuras que pueden transformar nuestras vidas de maneras que apenas comenzamos a imaginar.






Deja una respuesta