
La importancia de la energía de activación en las reacciones químicas
La energía de activación es un concepto fundamental dentro de la química que se refiere a la cantidad mínima de energía requerida para que una reacción química ocurra. Este fenómeno es crucial para entender cómo y por qué las reacciones químicas tienen lugar en diferentes condiciones. Sin una adecuada energía de activación, las interacciones moleculares pueden no ser suficientes para que los reactivos se conviertan en productos, lo que a menudo limita la velocidad y el alcance de las reacciones. En este artículo, se explorará el concepto de energía de activación, su papel en las reacciones químicas, y cómo diferentes factores pueden influir en este fenómeno.
La energía de activación no solo es un aspecto teórico; tiene aplicaciones prácticas que impactan diversas áreas, como la bioquímica, la ingeniería química, y la farmacología. Por lo tanto, comprender este concepto es vital para científicos y profesionales que trabajan en campos relacionados con la química. En las siguientes secciones, discutiremos en detalle qué es la energía de activación, las diversas formas en que se puede afectar, y su relevancia en la práctica. Con este conocimiento, el lector podrá apreciar la complejidad y la belleza de las reacciones químicas que nos rodean en el día a día.
¿Qué es la energía de activación?
La energía de activación es un término que proviene de la cinética química. Se refiere a la cantidad mínima de energía que los reactivos deben adquirir para que se produzca una reacción química. En términos más simples, es el esfuerzo energético que deben llevar a cabo las moléculas para romper enlaces en los reactivos y formar nuevos enlaces en los productos. Esta energia se puede visualizar como una barrera que las moléculas deben superar. Cuanto más alta sea la energía de activación, más difícil será que las moléculas de los reactivos reaccionen entre sí.
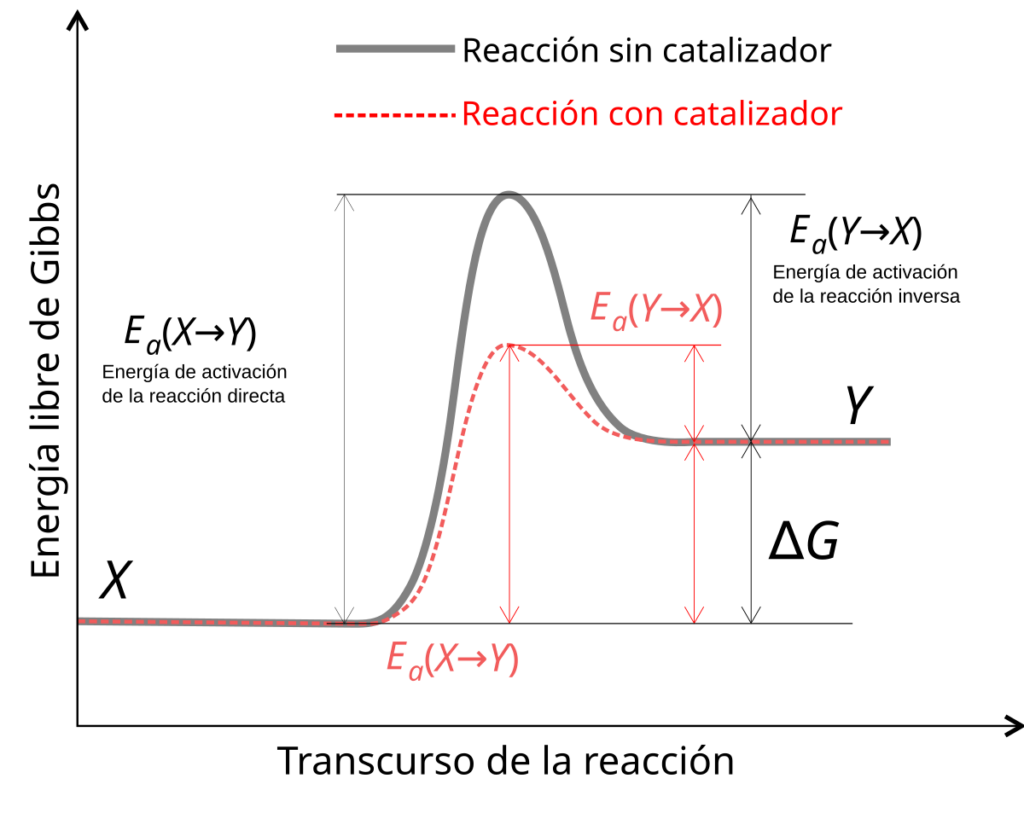
El concepto de energía de activación se ilustra comúnmente a través de un gráfico que muestra la energía en función del progreso de la reacción. Este gráfico presenta un pico que representa la energía de activación, donde los reactivos necesitan alcanzar este punto crítico antes de que puedan transformarse en productos. Por lo general, la energía de activación depende de la naturaleza de los reactivos, los productos que se forman y las condiciones ambientales donde se lleva a cabo la reacción.
Importancia en la química
La energía de activación juega un papel crucial en el rate de las reacciones químicas. Dado que una reacción no puede proceder sin que se alcance dicha energía, la comprensión de este concepto es fundamental para quien estudie o trabaje en química. Por ejemplo, en las reacciones biológicas, los enzimas actúan como catalizadores que reducen la energía de activación necesaria, permitiendo que las reacciones ocurran más rápidamente y a temperaturas más bajas.
Entender la energía de activación permite a los científicos manipular las condiciones de reacción para optimizar resultados. Un claro ejemplo es en la industria química, donde se pueden usar catalizadores para disminuir la energía de activación, aumentando así la velocidad de reacción y la eficiencia general del proceso.
Factores que afectan la energía de activación
Existen varios factores que pueden influir en la energía de activación de una reacción química. Entre estos se encuentran la naturaleza de los reactivos, las condiciones ambientales, y la presencia de catalizadores. Comprender estos factores es esencial, ya que ajustarlos puede llevar a cambios significativos en el comportamiento de una reacción química.
Naturaleza de los reactivos
La estructura y propiedades de los reactivos pueden tener un impacto importante en la energía de activación. Moléculas más complejas generalmente exhiben energías de activación más altas debido a las interacciones intrínsecas que deben superarse durante la reacción. Por ejemplo, en una reacción de oxidación, los enlaces de carbono en moléculas complejas pueden requerir mayor energía para romperse en comparación con reacciones que involucran compuestos simples.
Temperatura y presión
La temperatura y la presión son condiciones ambientales que pueden afectar la energía de activación. Al aumentar la temperatura, se incrementa la energía cinética de las moléculas, lo que significa que hay una mayor probabilidad de que las moléculas alcancen la energía necesaria para realizar la reacción. Igualmente, cambios en la presión pueden intensificar la densidad de las moléculas, favoreciendo la interacción entre reactivos. En general, estas condiciones contribuyen a facilitar el proceso de alcanzar la energía de activación requerida.
Catalizadores
Los catalizadores son sustancias que aumentan la velocidad de una reacción química al reducir la energía de activación necesaria. Los catalizadores actúan proporcionando un camino alternativo para la reacción que tiene una energía de activación más baja. Esto no solo acelera la reacción, sino que también permite que esta y otras reacciones ocurran en condiciones que serían inviable de otro modo, como a temperaturas más bajas. Ejemplos de catalizadores incluyen los enzimas en reacciones biológicas, que son cruciales para la vida y la función celular.
Aplicaciones de la energía de activación
La energía de activación tiene numerosas aplicaciones en diferentes campos, desde la industria química hasta la farmacología. Comprender cómo manipular esta energía puede llevar a procesos más eficientes y la creación de productos más efectivos. Por ejemplo, en la fabricación de medicamentos, la forma en que los reactivos se combinan debe ser cuidadosamente monitoreada para asegurar que se superen las energías de activación adecuadas, todo mientras se reduce el tiempo de reacción.
Otra aplicación se encuentra en la catálisis industrial, donde los catalizadores permiten que las reacciones necesarias para producir energía y productos químicos se realicen más efectivamente. Gracias a la reducción de la energía de activación, los procesos pueden desarrollarse a temperaturas más bajas, lo que ayuda a reducir costos y a minimizar el impacto ambiental al disminuir la emisión de gases de efecto invernadero.
Conclusión
La energía de activación es un concepto clave que influye en la comprensión de las reacciones químicas. No solo se trata de una barrera energética, sino que también desempeña un papel vital en la forma en que los científicos y profesionales manipulan los procesos químicos en sus respectivas disciplinas. La capacidad de entender y controlar la energía de activación tiene importantes implicaciones prácticas, desde la creación de eficientes sistemas industriales hasta la optimización de procesos biológicos.
A medida que continuamos explorando más sobre este concepto, se hace evidente que sigue siendo un área de estudio vasto y emocionante que influye en el futuro de la ciencia y la tecnología. Las metodologías para manipular la energía de activación no solo enriquecerán la química como disciplina, sino que también ofrecerán soluciones innovadoras para problemas actuales y futuros que enfrenta nuestra sociedad. A través del avance en la comprensión de este concepto, es posible desencadenar nuevas reacciones que mejoren no solo nuestra calidad de vida, sino el desarrollo sostenible del planeta.




Deja una respuesta