
Es importante entender si energía y calor son lo mismo o no
- ¿Calor y Energía es lo Mismo? Descubriendo las Diferencias Clave
- Definición de Energía y Calor
- Diferencia entre Calor y Temperatura
- Interrelación entre Energía y Calor
- ¿Cuál es la Diferencia entre Calor y Temperatura en el Contexto Práctico?
- Conceptos Relacionados y Aplicaciones Prácticas
- Conclusión
¿Calor y Energía es lo Mismo? Descubriendo las Diferencias Clave
La relación entre la energía y el calor es un tema de gran relevacidad en la física y en diversas aplicaciones prácticas, desde la ingeniería hasta la biología. Ambos conceptos son fundamentales para comprender cómo funcionan muchos procesos en nuestro entorno, pero es crucial distinguirlos, ya que a menudo se utilizan indistintamente en conversaciones cotidianas. Por un lado, la energía se refiere a la capacidad de realizar trabajo o provocar un cambio, mientras que el calor se define como una forma de energía que se transfiere entre sistemas en función de la diferencia de temperatura. En esta exposición, se explorarán las distinciones entre ambos conceptos, sus interrelaciones y sus aplicaciones en la vida diaria.
Este artículo se divide en secciones que abarcan desde las definiciones básicas de energía y calor, hasta la forma en que interactúan y se manifiestan en diferentes contextos. A través de un análisis detallado, se espera que el lector obtenga una comprensión clara de cómo se diferencia cada término y por qué es fundamental no confundirlos. Así, se sentarán las bases para una discusión más amplia sobre temas relacionados, como la termodinámica, la conservación de la energía y la eficiencia energética. Con esta introducción, procederemos a definir cada uno de estos conceptos para establecer una base sólida para el resto del artículo.
Definición de Energía y Calor
La energía, en su forma más general, se puede entender como la capacidad de realizar trabajo. Esta puede presentarse en numerosas formas, tales como energía cinética, potencial, eléctrica, térmica, entre otras. En términos más específicos, la energía es un atributo de un sistema que permite realizar un trabajo o provocar un cambio en su estado. Es importante señalar que la energía no se puede crear ni destruir, sino que solo se transforma de una forma a otra, siendo esta una de las leyes fundamentales de la física, conocido como el principio de conservación de la energía.
Por otro lado, el calor es una forma particular de energía que, como hemos mencionado anteriormente, se transfiere entre sistemas debido a diferencias de temperatura. En términos técnicos, el calor se define como la transferencia de energía térmica que ocurre entre un cuerpo frío y uno caliente. Este proceso tiene lugar siempre que haya un gradiente térmico, lo que implica que el calor fluye en la dirección de mayor temperatura hacia la de menor temperatura. El calor se mide en unidades como calorías o joules y es un concepto crucial en la termodinámica.
La Distinción entre Energía Térmica y Calor
Es esencial no confundir la energía térmica con el calor. La energía térmica es la energía interna contenida en un sistema que resulta de la energía cinética de las partículas en movimiento. Cuantas más partículas se mueven y más rápido lo hacen, mayor es la energía térmica del sistema. Mientras que el calor se refiere a la energía transferida entre dos sistemas, la energía térmica se refiere a la energía que reside dentro de un sistema en equilibrio térmico. Por lo tanto, aunque ambos términos están relacionados, no son equivalentes.
Diferencia entre Calor y Temperatura
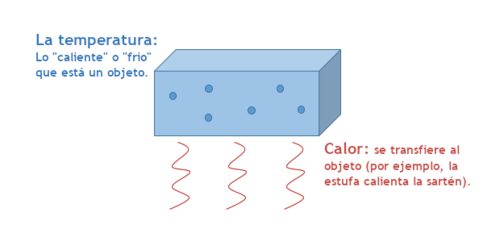
Comprender la diferencia entre calor y temperatura es vital en el estudio de la física y la termodinámica, así como en aplicaciones prácticas. La temperatura es una medida del grado de agitación térmica de las partículas de un cuerpo y es una magnitud que refleja cuán caliente o frío está un objeto. El calor, en cambio, es la energía que se transfiere de un cuerpo a otro debido a una diferencia de temperatura. Por tanto, calor y temperatura están estrechamente relacionados pero no son lo mismo. La temperatura puede considerarse como un indicador del estado térmico de un sistema, mientras que el calor es el proceso de transferencia de esa energía térmica.
Interrelación entre Energía y Calor
La interrelación entre energía y calor es compleja y se manifiesta en varias leyes de la termodinámica. En términos generales, cualquier transferencia de calor implica también un cambio en la energía de los sistemas en cuestión. Por ejemplo, cuando un sistema genera calor, esto puede traducirse en un incremento de la energía térmica de otro sistema. Este fenómeno es fundamental en aplicaciones tecnológicas, como motores térmicos, refrigeradores y sistemas de calefacción, donde se aprovechan estas interrelaciones para llevar a cabo trabajo útil.
La primera ley de la termodinámica afirma que la energía total del universo se mantiene constante. Esto significa que la energía de un sistema puede variar mediante la adición o eliminación de calor. Por lo tanto, cuando un sistema realiza trabajo, debe perder energía térmica equivalente, o lo contrario, al recibir calor, incrementa su energía interna. La energía calefaccionada se convierte así en un motor que impulsa el movimiento de sistemas mecánicos o eléctricos.
Ejemplos de Aplicación de la Energía y Calor
Existen numerosos ejemplos en los que la comprensión de la interacción entre energía y calor resulta crucial. A continuación, se presentan algunos casos que ilustran su interrelación:
- Calefacción y Refrigeración: Los sistemas de calefacción utilizan la energía térmica para aumentar la temperatura de un ambiente, mientras que los sistemas de refrigeración transfieren calor fuera de un espacio para mantener una temperatura baja.
- Máquinas Térmicas: Los motores de automóviles convierten el calor producido por la combustión del combustible en trabajo mecánico, ejemplificando cómo el calor puede ser transformado en energía útil.
- Paneles Solares: Estos dispositivos transforman la energía del sol en calor, que a su vez puede ser utilizado para generar electricidad o calentar agua, destacando la conversión de formas de energía.
¿Cuál es la Diferencia entre Calor y Temperatura en el Contexto Práctico?
La cual es la diferencia entre calor y temperatura se manifiesta claramente en escenarios prácticos. Por ejemplo, al tocar un objeto metálico en un día frío, sentimos que el metal está muy frío, aunque en realidad está a la misma temperatura del aire. Esto se debe a que el metal es un buen conductor del calor y transfiere rápidamente el calor de nuestra mano al metal, dándonos una sensación de frío. Por lo tanto, la temperatura es una propiedad intrínseca del metal, mientras que el calor es la energía en tránsito que sentimos al tocarlo.
Conceptos Relacionados y Aplicaciones Prácticas
Además de la distinción fundamental entre energía y calor, existen más conceptos relacionados que forman parte de la misma categoría temática. Por ejemplo, la entropía es un concepto crítico en el estudio de la termodinámica que describe el grado de desorden en un sistema. A medida que el calor se transfiere, la entropía de los sistemas involucrados suele aumentar, lo que tiene implicaciones significativas en la eficiencia de los procesos energéticos.
Las aplicaciones prácticas de la relación entre energía y calor son vastas y abarcan desde la industria hasta el hogar. En la construcción de edificios, por ejemplo, la planificación de la eficiencia térmica puede llevar a un consumo energético más bajo, lo que se traduce en menores costos operativos y reducción de emisiones. En la industria manufacturera, el control del calor en diversos procesos, como el enfriamiento y la calefacción, es fundamental para garantizar la calidad y el rendimiento del producto final.
Importancia de la Eficiencia Energética
El concepto de eficiencia energética está intrínsecamente relacionado con la interacción entre energía y calor. La eficiencia se refiere a la capacidad de un sistema para convertir la energía utilizada en trabajo útil. Una mayor eficiencia implica que se utiliza menos energía para realizar el mismo trabajo, lo que se traduce en menor gasto económico y menor impacto ambiental.
Conclusión
Es imprescindible comprender que aunque la energía y el calor están intrínsecamente relacionados, no son equivalentes. La energía representa la capacidad de realizar trabajo, mientras que el calor es una forma de energía transferida entre sistemas a través de diferencias de temperatura. Esta distinción es crucial para cualquier aplicación práctica, desde la ingeniería hasta la biología. Además, conceptos adicionales como la eficiencia energética y la entropía son necesarios para entender cómo operan estos fenómenos en la realidad.
A medida que la sociedad continúa avanzando hacia tecnologías más sostenibles y eficientes, la comprensión de la energía y el calor será más importante que nunca. La capacidad de optimizar el uso de estos recursos no solo es vital para la economía, sino también para la conservación del medio ambiente. Entender la diferencia entre calor y temperatura y reconocer las diferencias entre calor y temperatura es, por lo tanto, un primer paso crítico, que nos permitirá tomar decisiones informadas sobre el uso de estos recursos en el día a día y contribuir a un futuro más sostenible.






Deja una respuesta