
De qué depende la energía interna de un gas en diferentes condiciones
La energía interna de un gas es un concepto fundamental en la termodinámica que se refiere a la energía total contenida dentro del sistema. Está estrechamente relacionada con la temperatura, el volumen y la cantidad de sustancia de un gas. Comprender qué factores determinan la energía interna de un gas no solo es vital para el estudio académico de la física y la química, sino también para la aplicación práctica en múltiples campos como la ingeniería, la meteorología y la climatización. Este artículo explora los componentes clave que influyen en la energía interna de un gas, con el fin de ofrecer una visión clara y detallada sobre su comportamiento y cambios en diversas condiciones.
Un punto relevante a tener en cuenta es que la energía interna de un gas ideal, por ejemplo, se relaciona directamente con la temperatura y es independiente del volumen y la presión, siempre que se mantenga constante la cantidad de sustancia. Sin embargo, en los gases reales, otros factores como las interacciones moleculares también juegan un papel crucial y no deben ser ignorados. A través de un análisis comprensivo de estos elementos, se busca ofrecer un artículo que no solo informe, sino que también fomente un entendimiento más profundo de los principios de la termodinámica relacionados con gases.
Temperatura y su Influencia en la Energía Interna
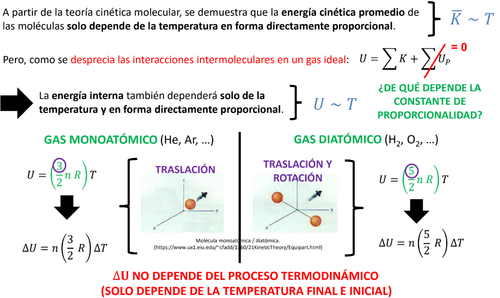
Uno de los factores más decisivos en la energía interna de un gas es la temperatura. En la termodinámica, la temperatura es una medida de la energía cinética promedio de las moléculas del gas. A medida que la temperatura de un gas aumenta, las moléculas se mueven más rápidamente, lo que incrementa su energía cinética. Por lo tanto, se puede establecer que hay una relación directa entre la temperatura y la energía interna de un gas. Esto es válido tanto para gases ideales como para gases reales, aunque en estos últimos la relación puede verse afectada por interacciones moleculares a altas temperaturas.
Relación Directa entre Temperatura y Energía Interna
La siguiente fórmula general representa la dependencia de la energía interna en función de la temperatura:
U = n C_v T
donde U es la energía interna, n es la cantidad de sustancia, C_v es la capacidad calorífica a volumen constante, y T es la temperatura en Kelvin. Esta ecuación implica que, a mayor temperatura, se incrementa la energía interna del sistema, siempre que el volumen se mantenga constante.
Efectos de las Interacciones Moleculares
En gases reales, las interacciones entre moléculas pueden influir en la energía interna. Por ejemplo, en condiciones de alta presión y baja temperatura, las fuerzas intermoleculares se vuelven significativas, lo que puede afectar el comportamiento termodinámico del gas. Las interacciones a nivel molecular pueden hacer que la energía interna sea menor que la predicha por la teoría de gases ideales, ya que las moléculas tienden a atraer y repeler entre sí. Este efecto es más notable en gases que tienen moléculas más grandes o polarizadas.
Cantidad de Sustancia y su Efecto
Otro factor crucial que determina la energía interna de un gas es la cantidad de sustancia presente en el sistema, generalmente expresada en moles. A medida que se incrementa la cantidad de sustancia, también aumenta la energía interna total del sistema. Este incremento se debe a la adición de más moléculas que contribuyen a la energía cinética total. Así, se confirma que la cantidad de sustancia, al ser un factor directamente proporcional a la energía interna, juega un papel fundamental en la configuración de la misma.
Capacidad Calorífica a Volumen Constante
La capacidad calorífica a volumen constante, representada por C_v, es otra variable que afecta cómo la energía interna responde a cambios en la temperatura. Cada gas tiene su propia capacidad calorífica específica. Por lo tanto, al añadir calor a un sistema a volumen constante, la variación en la energía interna no será la misma para todos los gases. Gases con alta capacidad calorífica requerirán más energía para experimentar el mismo incremento en su energía interna en comparación con aquellos con baja capacidad calorífica.
Ejemplo Práctico de la Relación
Considerando un gas ideal, si tenemos un sistema cerrado en el que se aumenta la temperatura añadiendo calor, la energía interna del gas cambiará de acuerdo con:
ΔU = n C_v ΔT
En este sentido, un aumento de tan solo un mol de un gas ideal con una capacidad calorífica de 3R (donde R es la constante de los gases) a una variación de temperatura de 10 K, resultaría en un incremento considerable en la energía interna del sistema, permitiendo observar cómo estos conceptos se manifiestan de forma práctica.
Volumen y Presión en la Energía Interna de un Gas
Si bien la energía interna de un gas es principalmente dependiente de la temperatura y la cantidad de sustancia, también es relevante considerar el volumen y la presión en el que el gas se encuentra. Según la teoría de gases ideales, para un gas ideal a temperatura constante, el producto de la presión y el volumen se mantiene constante, lo que implica que estos dos parámetros no alteran la energía interna directamente. Sin embargo, en gases reales, la influencia de la presión y el volumen puede medirse a través de cambios en la temperatura y la cantidad de sustancia.
El Modelo de Gas Ideal y la Constancia de la Energía Interna
En el modelo de gas ideal, se establece que la energía interna es una función de la temperatura únicamente. En este contexto, los cambios en el volumen y la presión no deben influir en la energía interna, ya que cada molécula del gas se comporta como una partícula independiente y no está sujeta a interacciones significativas. Esto se traduce en la afirmación de que los cambios en el estado del gas que alteran la presión y el volumen no alteran directamente su energía interna, mientras se mantiene constante la temperatura.
Influencia de las Condiciones Reales
Sin embargo, al aumentar la presión en un gas real, las interacciones moleculares se vuelven significativas, contribuyendo a una disminución de la energía cinética promedio, lo que puede llevar a la conclusión de que a altas presiones, la energía interna podría verse afectada. Por lo tanto, aunque la teoría de los gases ideales establece que la energía interna depende exclusivamente de la temperatura, es fundamental tener en cuenta que las condiciones reales afectan la precisión de esta afirmación en aplicaciones prácticas.
Conclusión
La energía interna de un gas es un tema complejo que depende de múltiples factores, entre los cuales se destacan la temperatura, la cantidad de sustancia, y en menor medida, las condiciones de presión y volumen. La relación directa entre la energía interna y la temperatura se refleja claramente en los sistemas cerrados de gases ideales, donde las interacciones moleculares pueden ser despreciadas. Sin embargo, en gases reales, la influencia de las interacciones entre las moléculas se vuelve crítica, especialmente en condiciones extremas.
La comprensión de estos conceptos no solo es fundamental para el desarrollo académico, sino que también tiene aplicaciones prácticas en diversas disciplinas. Desde la ingeniería hasta la climatización o la meteorología, el conocimiento de cómo cada uno de estos factores influye en la energía interna de un gas es crucial para la formulación de soluciones efectivas y eficientes. A medida que se avanza en el estudio de la termodinámica, se vuelve evidente que un entendimiento sólido de estos principios es esencial para poder abordar los desafíos que se presenten en contextos relacionados con gases y energía.






Deja una respuesta