
Cómo se produce el cambio de energía durante una reacción química
El estudio sobre el cambio de energía que se produce en las reacciones químicas es esencial para comprender los procesos fundamentales que rigen la química y, por ende, la vida misma. La energía es un componente crucial en las reacciones químicas, ya que determina la dirección y la viabilidad de estas. En muchas ocasiones, una reacción no puede proceder sin un aporte inicial de energía, conocido como energía de activación. Por lo tanto, el conocimiento del cambio de energía permite a los científicos y tecnólogos optimizar una variedad de procesos, desde la síntesis de nuevos compuestos hasta la mejora de la eficiencia energética en diferentes industrias. Este artículo abordará las definiciones, los tipos de energía, los procesos exergónicos y endergónicos, así como la influencia de la temperatura en las reacciones químicas, proporcionando así una visión integral sobre este tema crucial en el ámbito químico y físico.
Definición y Tipos de Energía en Reacciones Químicas
La energía en una reacción química se refiere al cambio en la energía total del sistema al pasar de reactivos a productos. Este cambio puede ser positivo o negativo, indicando así si se libera energía al entorno o si se requiere un aporte externo de energía para que la reacción se lleve a cabo. Es importante destacar que la energía en este contexto se puede clasificar en varias categorías:
- Energía cinética: Relacionada con el movimiento de las moléculas en el sistema.
- Energía potencial: Asociada a la posición de las moléculas y enlaces químicos dentro de los reactivos y productos.
- Energía interna: La suma de las energías cinéticas y potenciales de todas las partículas presentes en un sistema.
- Energía de activación: Mínima cantidad de energía necesaria para iniciar una reacción química.
La comprensión de estos tipos de energía es fundamental para el análisis de cómo y por qué ocurren ciertas reacciones. La transformación energética en una reacción es dinámica y se refleja en las propiedades físico-químicas de los compuestos involucrados. A menudo, las reacciones químicas pueden clasificarse en dos categorías principales basadas en el cambio de energía que producen.
Reacciones Exergónicas
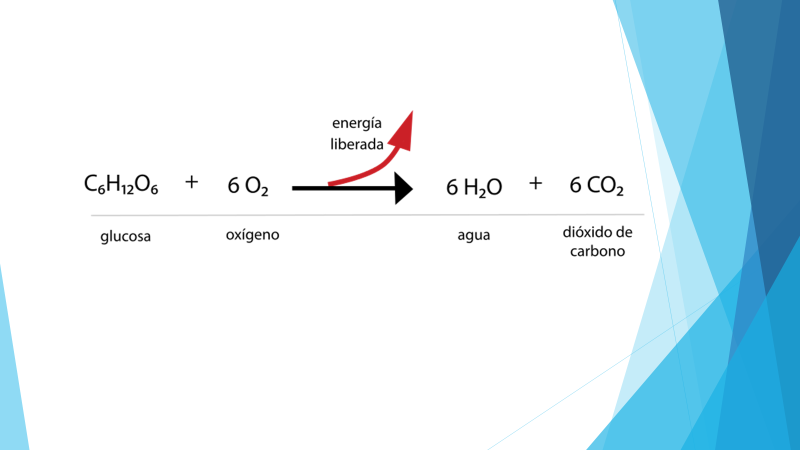
Las reacciones exergónicas son aquellas que liberan energía al entorno una vez que se han llevado a cabo. Esto significa que la energía potencial de los productos es menor que la de los reactivos. Un ejemplo clásico de reacciones exergónicas son la combustión de los hidrocarburos, donde se produce calor y luz, y la energía liberada se puede utilizar para realizar trabajo. Estas reacciones son spontaneas y suelen estar asociadas con procesos que generan calor, que se conocen como reacciones exotérmicas. En estas reacciones, el cambio de energía es negativo, lo que implica que el sistema pierde energía al medio ambiente.
Reacciones Endergónicas
Por otro lado, las reacciones endergónicas son aquellas que requieren un aporte de energía para que puedan tener lugar. Esto se observa en procesos como la fotosíntesis, donde las plantas absorben energía solar para convertir dióxido de carbono y agua en glucosa y oxígeno. En este caso, la energía de los productos es mayor que la de los reactivos, y el cambio de energía es positivo. Las reacciones endergónicas son importantes en sistemas biológicos donde la acumulación de energía es necesaria para la formación de compuestos complejos, y generalmente se vinculan con procesos que consumen calor, como las reacciones endotérmicas.
Influencia de la Temperatura en las Reacciones Químicas
La temperatura juega un papel crucial en la energía de las reacciones químicas. A medida que aumenta la temperatura, se incrementa la energía cinética de las moléculas, lo que generalmente conduce a un aumento en la velocidad de reacción. Esto se debe a que las moléculas se mueven más rápidamente, lo que resulta en un mayor número de colisiones efectivas entre ellas. Estas colisiones deben tener suficiente energía para superar la energía de activación requerida para que la reacción tenga lugar. Por lo tanto, un aumento en la temperatura puede hacer que una reacción exergónica ocurra más rápidamente y que una reacción endergónica se lleve a cabo más fácilmente.
Efectos en la Velocidad de Reacción
Un aumento de la temperatura suele aumentar la tasa de las reacciones químicas. Este comportamiento se puede observar en diversas reacciones, desde la descomposición de sustancias hasta las reacciones de síntesis. Sin embargo, es importante observar que no todas las reacciones responden de la misma manera al cambio de temperatura; algunos procesos pueden presentar un óptimo de temperatura donde se logra la máxima eficiencia antes de empezar a decaer. Esto se debe a la posible descomposición de reactivos o productos, que puede llevar a la ineficacia de la reacción. Por lo tanto, el control de temperatura no solo es crucial para maximizar la tasa de reacción, sino también para asegurar la estabilidad de los compuestos involucrados.
Principio de Le Chatelier
El principio de Le Chatelier es un concepto fundamental que regula cómo las reacciones químicas responden a cambios en las condiciones. Este principio establece que si un sistema en equilibrio se ve afectado por un cambio en las condiciones (como temperatura, presión o concentración), el sistema siempre reaccionará de tal manera que minimice el efecto del cambio. Por lo tanto, al manipular la temperatura, se puede influir en la dirección de la reacción y en el equilibrio entre reactivos y productos, dependiendo de si la reacción es exotérmica o endotérmica.
Calculando el Cambio de Energía en Reacciones Químicas
El cálculo del cambio de energía en una reacción química se basa en la aplicación de la ley de conservación de la energía, lo que implica que la energía total de los reactivos y productos puede ser comparada para determinar el cambio energético. Una forma común de calcular este cambio de energía es mediante el uso de las entalpías de formación estándar de los reactivos y productos. La entalpía es una medida de la energía total de un sistema en condiciones de presión constante.
La fórmula que se utiliza comúnmente es:
ΔH = ΣH(productos) - ΣH(reactivos)
Donde ΔH representa el cambio de entalpía, ΣH(productos) es la suma de las entalpías de formación de los productos, y ΣH(reactivos) es la suma de las entalpías de formación de los reactivos. Este cálculo permite a los científicos predecir la espontaneidad de una reacción química, así como su comportamiento bajo diferentes condiciones. Un ΔH negativo indica que la reacción es exergónica y libera energía, mientras que un ΔH positivo indica que la reacción es endergónica y requiere energía para llevarse a cabo.
Conclusión
El cambio de energía en las reacciones químicas es un concepto multifacético que no solo involucra la cantidad de energía liberada o absorbida, sino que también está profundamente interrelacionado con las condiciones de la reacción como la temperatura y la concentración. Comprender este cambio energético es esencial para aplicar la química en múltiples campos, ya sea en la industria, en la biología o en la investigación científica. La capacidad de predecir cómo una reacción se comportará bajo distintas condiciones permite optimizar procesos, mejorar la eficiencia energética y contribuir al desarrollo de tecnologías novedosas. La investigación sobre el cambio de energía proporciona las bases necesarias para el avance en diversas aplicaciones químicas y materiales. Por lo tanto, una sólida comprensión de estos procesos es vital para la ciencia moderna y su aplicación en el futuro.




Deja una respuesta