
Cómo funcionan las letras para representar los subniveles de energía en la estructura atómica
La estructura atómica es un pilar fundamental de la química y la física moderna, proporcionando un contexto esencial para entender cómo se organizan los electrones en los átomos. En este contexto, los subniveles de energía juegan un papel crucial, ya que determinan cómo y por qué los electrones se distribuyen en distintos niveles y subniveles de energía. A medida que se avanza en el estudio de la teoría atómica, es esencial comprender la notación utilizada para representar estos subniveles, que se designan mediante letras y números. Este artículo explorará en detalle las letras que representan los subniveles de energía y su significado dentro de la teoría cuántica, así como la manera en la que estas representaciones influyen en la formación de elementos y compuestos químicos.
Para abordar este tema, comenzaremos explicando cómo se estructuran los niveles de energía en un átomo inicial, y luego nos adentraremos en la representación específica de cada subnivel. La notación utilizada no solo simplifica la comunicación de conceptos complejos, sino que también facilita la comprensión del comportamiento electrónico. Al final, destacaremos la importancia de esta representación en la química moderna y su aplicación práctica en diversas áreas de estudio, desde la biología hasta la ingeniería. Con esta base, podremos contextualizar la función de los subniveles y su representación de manera efectiva.
Estructura de los niveles de energía en los átomos
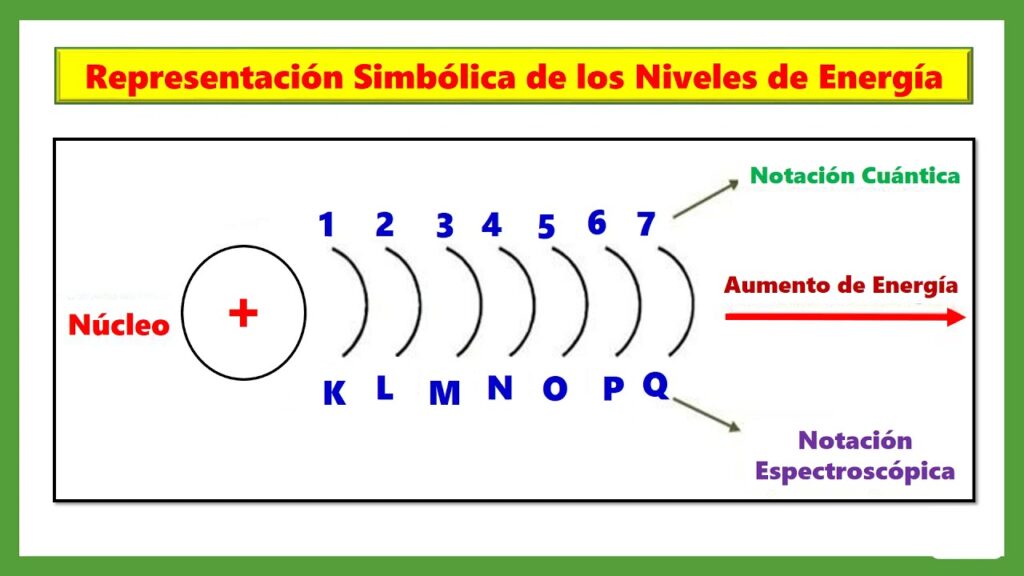
Los átomos están constituidos por un núcleo central rodeado por electrones que orbitan en diferentes niveles de energía. Estos niveles de energía se pueden clasificar entre sí, y esta clasificación se basa en el principio de Cuantización, propuesto por Max Planck y Albert Einstein. Cada uno de los niveles de energía corresponde a un número cuántico principal (n), que toma valores enteros positivos (1, 2, 3, etc.). Cuanto mayor es el número cuántico principal, mayor es la distancia del electrón respecto al núcleo y, por ende, su energía.
Dentro de cada uno de estos niveles de energía, existen varios subniveles. Los subniveles son regiones dentro de cada nivel principal donde es posible encontrar electrones con energías similares. Es preciso entender que no solo se denomina a los niveles de energía con números, sino que también se utilizan letras para identificar los subniveles asociados a cada uno. Las letras utilizadas para representar estos subniveles son: s, p, d y f. Cada letra representa una forma característica de la nube de electrones, lo cual influye en la manera en que los átomos interactúan entre sí.
Subniveles de energía y sus letras correspondientes
Los subniveles de energía se clasifican en función de su forma y capacidad para albergar electrones. En la actualidad, se reconocen cuatro tipos principales de subniveles, identificados por letras específicas. A continuación, se describen brevemente estas letras y sus características inherentes:
- s: Cada subnivel s puede contener hasta 2 electrones. Su forma es esférica y es el subnivel más bajo en energía dentro de cada nivel.
- p: Los subniveles p pueden albergar hasta 6 electrones. Tienen forma de lóbulos y suelen organizarse en grupos de tres, formando un modelo simétrico alrededor del núcleo.
- d: Este subnivel puede contener hasta 10 electrones. La forma de los orbitales d es más compleja, presentando cinco orientaciones distintas.
- f: Por último, el subnivel f puede alojar hasta 14 electrones. Los orbitales f son los más energéticamente costosos y tienen formas aún más complicadas que los subniveles anteriores.
Importancia de la notación de los subniveles de energía
La notación de los subniveles de energía es fundamental para comprender la química detrás de la formación de átomos y sus interacciones. Cada elemento en la tabla periódica se caracteriza por su número atómico, que indica la cantidad de protones en su núcleo y, en un átomo neutro, también el número de electrones. Estos electrones se distribuyen en los niveles y subniveles de energía de acuerdo con el principio de Aufbau, el principio de Pauli y la regla de Hund. Estas reglas estipulan cómo se ocupan los subniveles de energía, priorizando la configuración que minimiza la energía total del átomo.
Por ejemplo, la configuración del hidrógeno (H) se representa como 1s1, donde el número 1 indica el primer nivel de energía y la letra s representa el subnivel correspondiente, que en este caso tiene un solo electrón. Cuando se consideren elementos más complejos como el carbono, la configuración se verá como 1s2 2s2 2p2, lo que demuestra la forma en la que los electrones se distribuyen en niveles cada vez más altos. Esta representación no solo es fundamental para la comprensión atómica, sino que también influye en las propiedades químicas de un elemento, como su reactividad y valentía. Por lo tanto, comprender el significado y la importancia de estas letras es indispensable para el estudio avanzado de la química y la física.
Relevancia en la formación de enlaces químicos
La representación de los subniveles de energía también condiciona cómo los átomos se unen para formar compuestos. Las interacciones químicas se producen generalmente a través del intercambio o compartición de electrones en los subniveles de más alta energía, conocidos como electrones de valencia. Por ejemplo, en los metales de transición, donde los orbitales d están parcialmente ocupados, la forma en que estos electrones influyen en la estructura y propiedades del material es crucial. La capacidad de un elemento para formar enlaces covalentes o iónicos depende fuertemente de la configuración de sus electrones de valencia, que a su vez está determinada por la notación de los subniveles.
Aspectos clave sobre la representación de subniveles de energía
La representación de los subniveles de energía tiene varios aspectos clave que son importantes considerar para una comprensión más profunda de la estructura atómica. Estos aspectos nos brindan una perspectiva integral sobre cómo interactúan y se organizan los electrones en los átomos.
- Distribución y organización: La forma en que los electrones se distribuyen en los subniveles puede influir en las propiedades físicas y químicas de los elementos y compuestos.
- Interacción y enlace: La capacidad de formar enlaces químicos depende de la configuración electrónica de valencia, que a su vez está determinada por la distribución en los subniveles.
- Efectos en la reactividad: La estabilidad de los electrones en los subniveles influye directamente en la reactividad de los elementos, afectando el modo en que participan en reacciones químicas.
Conclusión sobre los subniveles de energía y sus letras
La notación de los subniveles de energía, utilizando letras como s, p, d y f, es un componente fundamental en la comprensión de la estructura atómica y el comportamiento de los electrones. A través de esta notación, es posible representar de manera efectiva la organización de los electrones en los diferentes niveles de energía, lo cual es esencial para analizar la composición de los elementos. Cada letra no solo representa un subnivel específico, sino que también refleja la capacidad de ese subnivel para albergar electrones, lo que tiene un impacto crucial en las propiedades químicas de los elementos.
Conocer la estructura de niveles y subniveles de energía ayuda a los estudiantes y profesionales de la química y la física a comprender la interacción de los átomos en compuestos y su comportamiento en diversas reacciones. La implementación de esta representación es indispensable no solo en el ámbito académico, sino que también tiene aplicaciones prácticas en campos como la medicina, la biología, la ingeniería, y muchos otros. Por lo tanto, dominar la notación de los subniveles de energía es un paso esencial para avanzar en la comprensión de la ciencia detrás de la materia y sus interacciones, para posteriormente aplicar este conocimiento con fines diversos.



Deja una respuesta